
Die Qualität und Bedeutung wissenschaftlicher Studien werden häufig anhand des Studiendesigns und der Art und Weise beurteilt, in der ein statistischer Analyseplan Methoden zur Reduzierung des Risikos einer Verzerrung und unausgewogener Datensätze integriert hat. Hierzu gehören die Randomisierungsverfahren für Teilnehmer, die Einbeziehung geeigneter Kontrollgruppen, die Verwendung einer bewährten Methodik und die Rekrutierung einer beträchtlichen Stichprobengröße, um statistische Signifikanz zu erzielen. Allgemein kann eine randomisierte kontrollierte Studie gemäß den GRADE-Kriterien (Guyett et al., 2008) als Goldstandard-Studiendesign für interventionsbasierte Studien eingestuft werden.

Randomisierte Kontrollstudie vs. synthetischer Kontrollarm
Bei einem randomisierten kontrollierten Studiendesign (RCT) werden die Teilnehmer in zwei oder mehr Gruppen aufgeteilt, typischerweise eine Interventionsgruppe (Medikament, Bewegung oder Therapie) und eine Kontrollgruppe, die eine Placebo- oder Standardbehandlungsgruppe sein kann. Im Zusammenhang mit der Onkologie Interventionen mit einer Kontrollgruppe über verschiedene Studien hinweg haben zu einem enormen Anstieg der Kosten klinischer Studien geführt und die Notwendigkeit verdeutlicht, alternative Lösungen zu finden.
Eine weitere wichtige Überlegung für das RCT-Studiendesign und den erfolgreichen Abschluss einer RCT für das untersuchte Medikament oder die untersuchte Behandlung ist ob die Teilnehmer nicht bereit sind, sich den neuen Medikamentenkandidaten verabreichen zu lassen, der ihre Krankheit möglicherweise heilen könnte, die bereit sind, an der Studie teilzunehmen, auch wenn sie zu dieser Kontrollgruppe gehören. Dies kann zu höheren Abbruchquoten führen, was wiederum das Risiko einer Verzerrung mit sich bringt, die statistische Aussagekraft der Studie verringert und die Dauer der Studie verlängert, was erhebliche finanzielle Folgen hat (Groth 2010).
Eine aus Patientendaten abgeleitete synthetische Kontrollgruppe könnte eine neuartige und kostengünstige Lösung für diese Probleme bieten. Bei seltenen Krankheiten oder immer komplexeren Krankheitsphänomenen kann dies die erfolgreiche Durchführung klinischer Studien ermöglichen (Thorlund et al., 2020). Dieser auf der Generierung von Real-World Evidence (RWE) basierende Ansatz wird von der US-amerikanischen Food and Drug Agency (FDA), der Europäischen Medizinagentur (EMA) und dem National Institute for Clinical Excellence im Vereinigten Königreich unterstützt.
Durch die Verwendung eines synthetischen Kontrollarms und fortschrittlichen Data-Minings wie künstliche Intelligenz (KI) in medizinischen Bildgebungstechnologien, bietet die Möglichkeit, die Dauer klinischer Studien rasch zu verkürzen, ihre Durchführbarkeit zu erhöhen, sie finanziell tragfähiger zu machen und eine verzerrte Berichterstattung zu verringern.
Was ist ein synthetischer Querlenker?
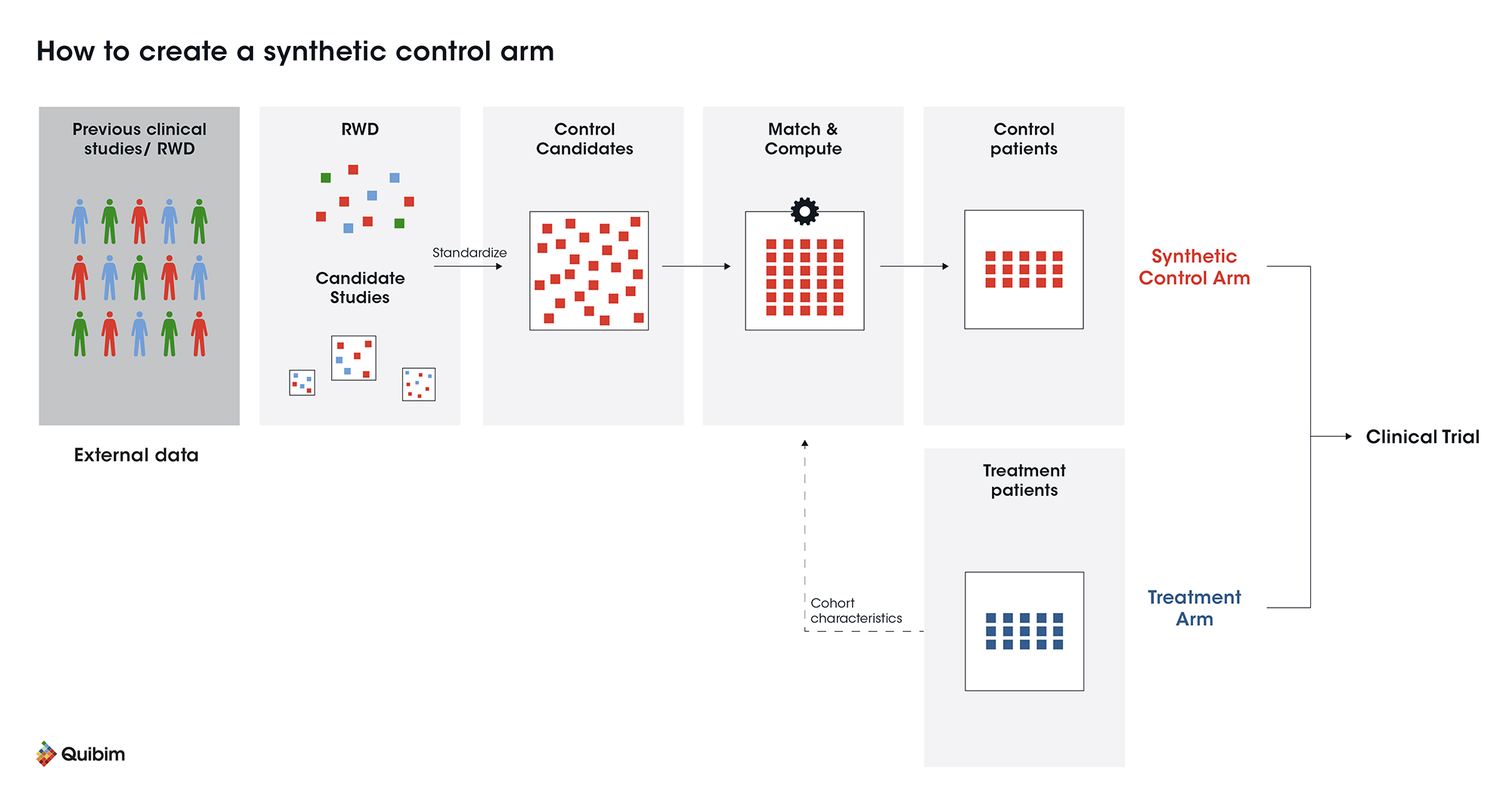
Mit der Methode der synthetischen Kontrolle kann die Wirksamkeit einer Intervention anhand externer Kontrolldaten verglichen werden. Der synthetische Kontrollarm kann als unabhängige Kontrollgruppe oder als Adjuvans zu einer Kontrollgruppe hinzugefügt werden. Externe Kontrollarmdaten können in erster Linie aus Beobachtungsdaten, Realweltdaten (RWD) und Daten aus früheren klinischen Studien abgeleitet werden. Die Gültigkeit und Robustheit dieses Ansatzes wurde bereits angemessen analysiert und akzeptiert (Thorlund et al., 2020).
Der größte Vorteil einer synthetischen Kontrollgruppe ergibt sich, wenn gemäß Stichprobengrößenberechnungen nur wenige Patienten mit spezifischen Einschlusskriterien erforderlich sind, um mutmaßliche Unterschiede zwischen der neuen Behandlung und der Standardbehandlung zu bewerten. In diesem Szenario wäre es unpraktisch, zeitaufwändig und teuer, geeignete Patienten für die Kontrollgruppe zu finden. Eine synthetische Kontrollgruppe kann diese Probleme möglicherweise lösen.
Der erfolgreiche Einsatz eines synthetischen Arms hängt von der Qualität der verwendeten Daten ab, die für jede Studie spezifisch ist. Bei der Auswahl dieser Strategie sollten Sie unter anderem folgende Aspekte berücksichtigen:
-
Ist die Kontrollgruppe für die untersuchte Population relevant?
-
Was ist die Quelle der synthetischen Kontrollgruppe?
-
Wie wird die synthetische Kontrollgruppe der Interventionsgruppe zugeordnet?
-
Sind die Populationen der neuen Behandlungsgruppe und der synthetischen Kontrollgruppe ähnlich? Zu den Faktoren zählen ethnische Zugehörigkeit, sozioökonomisches Umfeld, körperliche Aktivität und geografische Region.
-
Handelt es sich um eine ausreichende Stichprobengröße und wurde die entsprechende Anzahl an Kovariablen/Störfaktoren gemessen?
-
Wie ist im Fall von adjuvanten synthetischen Kontrollgruppen das Hybridverhältnis zwischen synthetischen und „normalen“ Kontrollen?
-
Spiegelt die übliche Versorgung auf der Grundlage synthetischer Kontrolldaten die aktuelle klinische Praxis und Praxis der Bildgebung wider?
-
Stimmen die in den synthetischen Kontrollgruppen verwendeten Protokolle zur medizinischen Bilderfassung weitgehend mit denen überein, die bei den Untersuchungen der Interventionsgruppen angewendet wurden?
Jede dieser Überlegungen beeinflusst die Gültigkeit der Verwendung synthetischer Kontrollgruppen. Eine Berichterstattung darüber, wie sich dies auf die Ergebnisse auswirken kann, kann als bewährte Vorgehensweise angesehen werden. Maschinelles Lernen kann die Qualität und Validität dieser Gruppen erhöhen. Die Verwendung synthetischer Kontrollarme nimmt zu, einschließlich der jüngsten Phase-II/III-Onkologiestudien mit Daten aus den Studien MAMMOTH und SCHOLAR-1 (Banerjee et al., 2022).
Außerdem sind Einige Studien, die einen externen Kontrollarm als unterstützende Analyse verwendeten, ermöglichten eine beschleunigte behördliche Zulassung des Arzneimittels. (d. h. Blinatumomab für Patienten mit akuter lymphatischer Leukämie vom Vorläufer-B-Zelltyp in vollständiger Remission mit nachweisbarer minimaler Resterkrankung, BLAST-Studie) (Gökbuget N et al., 2018)
Externer Querlenker vs. synthetischer Querlenker
Während wir uns entwickelt haben, Externe und synthetische Kontrollarme sind alternative Ansätze, die in klinischen Studien verwendet werden, um die Wirksamkeit einer Intervention zu vergleichen, ohne immer auf eine traditionelle Kontrollgruppe zurückgreifen zu müssen. Obwohl beide Methoden darauf abzielen, die Anzahl der in der Kontrollgruppe benötigten Patienten zu reduzieren, liegen die Unterschiede in der Auswahl und Verwendung der Kontrolldaten:
Ein externer Kontrollarm besteht aus tatsächlichen Daten von Patienten, die an früheren klinischen Studien teilgenommen haben oder unter normalen klinischen Bedingungen behandelt wurden. Diese Daten stammen in der Regel aus Krankenakten, realen Datenbanken oder früheren Studien. Durch die direkte Verwendung dieser Daten können die Forscher Patienten in der Interventionsgruppe mit denen vergleichen, die zuvor mit Standardbehandlungen oder Placebo behandelt wurden, und so die Bildung einer neuen Kontrollgruppe in der aktuellen Studie vermeiden. Dies beschleunigt den Studienprozess und kann Kosten senken, birgt jedoch das Risiko, dass die verwendeten Daten nicht genau den Merkmalen der aktuellen Population entsprechen, entweder weil sich die Behandlungsstandards weiterentwickelt haben oder weil es Unterschiede in der medizinischen Versorgung zwischen den Studien gibt.
Auf der anderen Seite, Der synthetische Kontrollarm generiert unter Verwendung fortschrittlicher statistischer Modelle eine künstliche Kontrollgruppe. Anders als bei der externen Kontrolle, bei der die Daten unverändert verwendet werden, kombiniert die synthetische Kontrolle verschiedene Datenquellen, darunter frühere Studien und reale Beobachtungsdaten, um eine Kontrollgruppe zu erstellen, die die Interventionsgruppe so genau wie möglich simuliert. Diese Modelle ermöglichen eine Anpassung an Patientenmerkmale wie Alter, Krankheitsstatus und andere demografische Faktoren, um die synthetische Gruppe mit der Gruppe vergleichbar zu machen, die die neue Behandlung erhält. Diese Flexibilität ist insbesondere bei Studien nützlich, bei denen es schwierig ist, eine ausreichende Zahl Patienten zu rekrutieren, beispielsweise bei seltenen Krankheiten oder bei Studien mit strengen Einschlusskriterien. Der Erfolg eines synthetischen Arms hängt jedoch in hohem Maße von der Qualität der verwendeten Daten und der Fähigkeit der Modelle ab, gültige Vergleiche zu erstellen. Wenn die Daten unzureichend sind oder die Anpassung nicht genau ist, kann die synthetische Kontrolle eine Verzerrung einführen oder keine zuverlässige Darstellung des tatsächlichen klinischen Verhaltens sein.
Beide Ansätze haben Vor- und Nachteile. Der externe Kontrollarm verwendet echte, gut dokumentierte Daten, ist aber möglicherweise nicht vollständig mit dem aktuellen Studienkontext vergleichbar, während der synthetische Arm mehr Flexibilität und Anpassungsfähigkeit bietet, allerdings auf Kosten einer größeren statistischen Komplexität und Abhängigkeit von der Datenqualität. Externe Kontrollarme sind häufiger, wenn ausreichend historische Daten verfügbar sind, während synthetische Arme in Situationen eingesetzt werden, in denen traditionelle Studien unpraktisch oder kostspielig wären. Beide Methoden werden zunehmend in Bereichen wie der Onkologie eingesetzt, wo der Bedarf an schnelleren und kostengünstigeren Tests von entscheidender Bedeutung ist.
Welche Rolle spielen quantitative Bildgebung und KI in synthetischen Kontrollarmen?
Die Analyse der Endpunkte klinischer Studien anhand medizinischer Bildgebung stellt eine Herausforderung für die Gewährleistung der Konsistenz der Untersuchungsprotokolle zwischen den beteiligten Institutionen dar. Klinische Bildgebungsverfahren weisen eine große Bandbreite an Erfassungsparametern auf, wie etwa räumliche Bildauflösung, Kontrastmittelgabe, kVp und mAs (unter anderem) für die Computertomographie (CT), Echozeit, Wiederholungszeit und viele andere Sequenzparameter für die Magnetresonanztomographie (MRI). Darüber hinaus bieten verschiedene Anbieter unterschiedliche Rekonstruktionsalgorithmen an.
Alle diese Variablen, bekannt als „Scannereffekte“, können die Erkennung biologischer und pathologischer Informationen behindern. Bei der MRT ist dieses Problem noch ausgeprägter, da es keine standardisierte Intensitätsskala gibt. Daher muss bei RCTs die zentrale Verwaltung und Kontrolle der Angemessenheit medizinischer Bildgebungsuntersuchungen und ihrer Eignung im Hinblick auf das Studienprotokoll sorgfältig durch zentrale Leselabore (auch als Bildgebungskernlabore bezeichnet) erfolgen.
Der Fortschritt hin zur Verwendung synthetischer Kontrollgruppen in klinischen Studien erfordert systematischere Techniken, um die Patienten genau zu finden, die am besten zur synthetischen Kontrollgruppe passen. Mithilfe von KI können Patienten in Krankenhaus-Bilddatenbanken identifiziert werden, die ähnliche Bildgebungsprotokolle verwenden (durch automatische Generierung eines Ähnlichkeitsscores basierend auf DICOM-Dateimetadaten) wie die im Behandlungsarm der Studie benötigten. Darüber hinaus kann die KI-basierte Harmonisierungslösung integriert werden, um die großen Unterschiede zwischen den Bildern zu bewältigen, die aus verschiedenen Bildgebungszentren mit einer großen Bandbreite an Erfassungsparametern stammen.
Der Einsatz von selbstüberwachtem Lernen als Paradigmenwechsel in der KI, bei dem Modelle ohne Grundwahrheit lernen, ist für dieses Problem perfekt geeignet, da ein Modell durch Lernen der verschiedenen Muster zwischen den Bildaufnahmeparametern (Metadaten) und der resultierenden Bildqualität (Pixeldaten) generiert werden kann. Daher ermöglicht die Möglichkeit, scannerinvariante Darstellungen von Bilddaten (MR, CT, PET/CT) zur Extraktion harmonisierter Merkmale und Parameter als beste Grundwahrheitsausgaben aus der synthetischen Kontrollgruppe zu generieren, ohne dass relevante Bildinformationen verloren gehen oder verändert werden, trotz der inhärenten Unsicherheitsgrade eine kausale Schlussfolgerung aus realen Daten.
Außerdem sind Durch bildgebende Biomarker und die Extraktion von Radiomics-Merkmalen können Eigenschaften im Zusammenhang mit Angiogenese, Zelldichte, Tumorheterogenität, Aggressivität usw. quantifiziert werden. Die Quantifizierung dieser Indikatoren erfordert traditionell eine manuelle Abgrenzung der Anatomie oder von Läsionen, doch KI und Convolutional Neural Networks (CNN) automatisieren diese Analyse-Pipelines. Die erhaltenen quantitativen Merkmale können als virtuelle Gewebeprofilierungstechnologie betrachtet werden, um die externe Kontrollgruppe nicht nur auf allgemeiner Ebene abzugleichen, sondern auch nach ähnlichen Gewebesignaturen zu suchen.
Fazit
Jede Studie mit synthetischen Kontrollgruppen ist hinsichtlich der Generalisierbarkeit der Ergebnisse, der Interpretation und der zugehörigen statistischen Methodik mit eigenen Herausforderungen und Einschränkungen verbunden. Die Nutzung der Fachkompetenz von Spezialisten in den Bereichen Daten und Bildgebung von Projektbeginn an kann dazu beitragen, die Gültigkeit und Reproduzierbarkeit dieser neuen Methodik zu verbessern. Die Einbeziehung hybrider Kontrollgruppen, die synthetische und traditionelle Kontrollgruppen mischen, bietet eine effektive, wirtschaftliche und patientenfreundliche Option für klinische Studien.
Referenzen
- Anderson M, Naci H, Morrison D, Osipenko L, Mossialos E. Eine Überprüfung der NICE-Bewertungen von Arzneimitteln 2000–2016 ergab Unterschiede bei der Feststellung der vergleichenden klinischen Wirksamkeit. J Clin Epidemiol. 2018;105:50–59.
- Banerjee, R, Shonali M, Kelkar AH, Goodman A, Prasad V und Mohyuddin GR. Synthetische Kontrollarme in Studien zu multiplem Myelom und diffusem großzelligem B-Zell-Lymphom. Br J Haematol. 2022;196 (5): 1274–1277.
- Gökbuget N, Dombret H, Bonifacio M, Reichle A, Graux C, et al. Blinatumomab für minimale Resterkrankung bei Erwachsenen mit akuter lymphatischer B-Zell-Vorläuferleukämie. Blood. 2018. April 5;131(14):1522-1531.
- Groth SW. Honorar oder Zwang: Einsatz von Anreizen für Teilnehmer an klinischer Forschung. JNY State Nurses Assoc. 2010;41(1):11.
- Guyatt GH, Oxman AD, Kunz R, Vist GE, Falck-Ytter Y, Schunemann HJ. Was ist „Qualität der Beweise“ und warum ist sie für Kliniker wichtig? BMJ (Klinische Forschungsausgabe). 2008;336(7651):995-998.
- Thorlund K, Dron L, Park JJH, Mills EJ. Synthetische und externe Kontrollen in klinischen Studien – Eine Einführung für Forscher. Clin Epidemiol. 2020; 12:457–467.
